RESUMEN
La implementación de métodos de conservación se hace indispensable para el es- tudio de microorganismos como hongos fitopatógenos. El objetivo del presente trabajo es evaluar el crecimiento radial de cepas de Pyricularia sp. conservadas en Papel de filtro y Glicerol como crioprotector, para ello se llevó a cabo un experi- mento en el Laboratorio de Biotecnología del Centro Multidisciplinario de in- vestigaciones Tecnológicas (CEMIT) con dos cepas de Pyricularia sp (066M y 067M) aisladas de Digitaria horizontalis y Brachiaria sp. respectivamente. Las cepas fueron inoculadas en medio Agar-Avena y mantenidas a condiciones controladas de luz y temperatura (25ºC) por 7 días. Posteriormente, se realizó su conservación por los siguientes métodos; Papel de filtro a -20ºC y Papel de filtro a -80ºC (con Glicerol). Para su Congelamiento con glicerol (80%v/v), las cepas de Pyricularia sp. se almacenaron a -80ºC. Luego de 12 meses de almacenamiento se proce- dió a la reactivación bajo condiciones controladas de luz y temperatura (25ºC). Se evaluó el crecimiento radial durante 15 días (las pruebas fueron realizadas por triplicado). Las cepas conservadas por los métodos de congelamiento a -80ºC no presentaron crecimiento durante las observaciones realizadas, Por el contrario, con la conservación en Papel de filtro a -20ºC pudo observarse crecimiento sin dife- rencias significativas entre las cepas. En conclusión, la de conservación sobre Papel de filtro a -20ºC puede ser implementada para la recuperación con éxito de cepas de Pyricularia sp.
INTRODUCCIÓN
La implementación de métodos de conservación se hace indispensable en las in- vestigaciones efectuadas con microorganismos como hongos o bacterias que gozan de interés económico al ser causantes de varias enfermedades en cultivos agrícolas (Ladino et.al. 2016). A la fecha se han desarrollado varias técnicas cuyo fin es la conservación de un material viable con caracteres casi inalterados y similares al cultivo inicialmente aislado. Estos métodos en base a factores como tiempo y ca- racterísticas fisiológicas del microorganismo se agrupan en métodos de corto y lar- go plazo y en métodos alternativos. (Parra et al, 2006, Pinzón & Gutierrez, 2009) Entre los métodos considerados de largo plazo, así denominados por el tiempo de conservación largo (hasta 30 años dependiendo del microorganismo) se encuen- tran la congelación, en la cual se utiliza un criprotector (glicerol, dimetilsulfoxido, leche descremada, glucosa, lactosa, manitol etc.), para mantener las células inalteradas y conservadas a baja temperatura (-20ºC a -140ºC) y la liofilización que es básicamente la deshidratación por sublimación del agua (Ladino et al. 2016). Los materiales liofilizados pueden ser conservados a temperaturas comprendidas entre los 18ºC y 25ºC. (Arencibia et al, 2014). Estos métodos requieren de equi- pamientos costosos para mantener las condiciones adecuadas, es por ello que la conservación a corto plazo y otros métodos alternativos podrían resultar eficaces para el propósito, pero presenta la desventaja que las células no pueden permanecer almacenadas indefinidamente. Entre las técnicas es posible citar al subcultivo de microorganismo, con la cual se mantiene la actividad metabólica conservando al organismo en medio de cultivo fresco y nutritivo a temperaturas comprendidas en- tre los 4ºC. La suspensión del material a conservar en agua destilada y estéril bajo las mismas condiciones es otra opción de conservación a corto plazo (Martínez et al, 2009). Cuando los métodos antes mencionados no representan una opción para emplear sobre el microorganismo, es posible emplear los métodos alternativos. Se basan en la paralización de las actividades metabólicas por desecación del agua que a diferencia con la liofilización (deshidratación celular) este método solo elimina el agua disponible para las células, es posible citar a la desecación en papel de fil- tro y sobre sustratos inertes (arena, silica gel, algodón, gelatina, vidrio, porcelana, alginato, sales etc.) (Godinez et al, 2008). Las temperaturas de almacenamientos son variadas, comprendidas entre 4ºC y -18ºC, pudiéndose almacenar incluso a
-80ºC si se emplea alginato como sustrato inerte. El objetivo del presente trabajo fue evaluar la viabilidad de cepas de Pyricularia sp. conservadas en dos métodos alternativos (papel de filtro y papel de filtro con glicerol como crioprotector) y en un método a largo plazo (congelamiento con glicerol como crioprotector).
METODOLOGÍA
El ensayo fue llevado a cabo en el Laboratorio de Biotecnología del Centro Multi- disciplinario de investigaciones Tecnológicas de la Dirección General de Investiga- ción Científica y Tecnológica de la Universidad Nacional de Asunción (CEMIT- DGICT-UNA). Se trabajó con dos cepas de Pyricularia sp. (066M y 067M) aisladas de Digitaria horizontalis y Brachiaria sp. respectivamente. Las cepas del hongo fueron sembradas en medio Agar-Avena y mantenidas a condiciones de luz y temperatura adecuadas para su crecimiento durante 7 días. Posteriormente, se realizó la conser- vación de los materiales por los siguientes métodos; Conservación en papel de filtro (PF) a -20ºC, para el cual fueron trasferidos explantes de cada cepa sobre papel de filtro estéril en medio Papa-Dextrosa-Agar en condiciones adecuadas para el creci- miento, 8 días después, el papel de filtro con las cepas crecidas, se secó a temperatura ambiente (25ºC), dentro de placas vacías y estériles para su posterior almacenamien- to a -20ºC y a – 80ºC con Glicerol (80% v/v) como crioprotector (PF-G80). Para la técnica de conservación por Congelamiento con glicerol (80%v/v) (CG80) como crioprotector a -80ºC, se transfirieron explantes de las cepas de Pyricularia sp. a tubos con glicerol (80% v/v) directamente desde el medio Agar-Avena. Las cepas fueron mantenidas bajo las condiciones de conservación durante 12 meses, posteriormente se procedió a la reactivación de las mismas en medio Agar-Avena bajo condiciones controladas de luz y temperatura (22ºC – 25ºC). Se evaluó el crecimiento radial en centímetros (cm) durante 15 días a intervalos de 5 días realizándose un total de tres observaciones. Se estimuló la esporulación realizando un raspado a la placa en cá- mara húmeda, manteniendo esta condición por tres días. Posteriormente se evalúo la presencia de esporas al Microscopio óptico.
RESULTADOS Y DISCUSIÓN
La reactivación de las cepas conservadas durante un año en tres métodos diferentes, arrojó resultados no esperados debido a que las cepas conservadas por los métodos de congelamiento a -80ºC (PF-G80 y G80) en donde se empleó Glicerol como criopro- tector no presentaron diámetro de crecimiento durante las observaciones realizadas a lo largo del ensayo (Figura 1), lo cual implica que el hongo ha perdido la viabilidad en el transcurso del tiempo y no pudo recuperarse. El glicerol o glicerina tiene la función de preservar la integridad celular a temperaturas muy bajas con la capacidad de atravesar la membrana celular y evitar así efectos perjudiciales del aumento en la concentración de soluto generado por el congelamiento del agua (Arencibia et al, 2008).
Figura 1. Evaluación de la reactivación de las cepas 066M y 067M de Pyricularia sp. en Agar-Avena por los métodos de conservación PF (A-D), PF- G80 (B-E) y G80(C-F), por triplicado cada 5 días por un intervalo de 15 días. San Lorenzo, Paraguay, 2017.

Se han realizado varios estudios y se lo ha catalogado como un compuesto no toxi- co para las células, sin embargo, es posible que la concentración empleada (80%v/v) en este trabajo en comparación con otros haya resultado toxica para el microor- ganismo (Malik, 1996, Ladino et al, 2016, Cárdenas, 2010). En base a esto no se puede descartar por completo la técnica empleando este crioprotector, más bien es indispensable realizar estudios para encontrar la concentración adecuada de glice- rol para su implementación dentro de la técnica de congelamiento.
Por el contrario, con la conservación en papel de filtro a -20ºC se pudo observar crecimiento en las dos cepas con características macromorfologicas de aspecto y textura de la colonia correspondiente al género del hongo fitopatógeno, tal como se observa en la figura 1 y tabla 1. Este método alternativo de conservación puede ser empleado con éxito para la recuperación de las cepas de Pyricularia sp.
Tabla 1. Crecimiento de las cepas de Pyricularia sp. Conservadas durante 12 meses en tres métodos diferentes; Papel de Filtro (PF), Glicerol 80% (G80) y una combinación de Papel de Filtro con Glicerol (PF-G80). Las cepas fueron reactivadas en Agar-Avena y evaluadas durante 15 días. San Lorenzo, Paraguay, 2017.
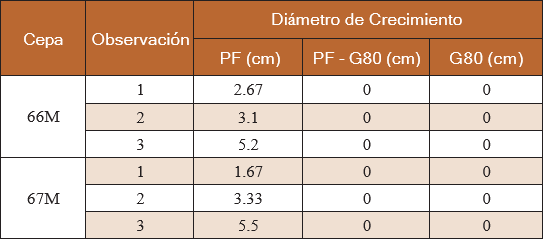
En cuanto a la esporulación, esta fue escasa en las condiciones provistas dentro de la cámara húmeda para ambas cepas, es posible que sea necesario ajustar algunos factores importantes como humedad elevada y la temperatura para estimular con éxito la esporulación.
CONCLUSIÓN
Los métodos de conservación (Congelamiento con crioprotector a -80ºC y el método alternativo generado por la combinación de papel de filtro y criopro- tector a -80ºC) resultaron inadecuados para la conservación de cepas de Pyricularia sp. Se hace necesario evaluar la concentración ideal del crioprotector para implementarlo dentro de las técnicas. La técnica alternativa de conserva- ción sobre papel de filtro a -20ºC puede ser implementada para la recuperación con éxito de cepas de Pyricularia sp.
REFERENCIAS BIBLIOGRÁFICAS
_ Arencibia, D. Fernández, L & Menéndez, R. 2008. Métodos generales de conservación de microorganismos. Finlay Ediciones. Colombia, p1 -14
_ Cárdenas, Y.; D. Rodríguez; O. Elósegui. 2010. Trichoderma harzianumRifai cepa A-34. Métodos de conservación y evaluación de sus formulados, tesis en opción al título de Licenciado en Microbiología, Facultad de Biología, Universidad de La Habana, Cuba.
_ Godinez, S. Calderón, M. 2008. Métodos Alternativos para la conservación de Hongos Filamentosos. Ciencia y Tecnología de Alimentos, Cuba, v 18 n2 p 31-37
_ Malik K.A. 1996Freezedrying of microorganismsusing a simple apparatus. TechnicalIn- formationfor Culture CollectionsCurators in DevelopingCountries. EducationCommit- tee. U/W, 29-32. K. A. Malik (ed), p 256-260
_ Martínez, A. León, M & González, G. 2009. Conservación de cepas de Candidauti- lis en agua destilada estéril. Instituto Cubano de Derivados de la Caña de Azúcar, Cuba, v XLIII n2 p 47-50
_ Ladino, E. Rubio, J &Chacin, C. 2016. Evaluación de dos métodos de conservación de hon- gos filamentosos patógenos de palma de aceite. Centro Agrícola, Colombia, v 43 n p 36-41
_ Parra, S. M. Pérez, M. Bernal. Z, Suares& D. Montoya.2006. Implementación y evalua- ción de dos métodos de conservación y generación de la base de datos del banco de cepas y genes del instituto de Biotecnología de la Universidad Nacional de Colombia, Colom- bia, v4 n5 p 1-116
_ Pinzón, A. Gutiérrez, Y. Bustamante, S. & Buitrago, S. 2009. Evaluación de métodos para la conservación de hongos fitopatógenos del ñame (Dioscoreasp.). Revista Colombiana de Biotecnología, Colombia, v XI n 2 p 8-18


 English
English